 Коррозия бетонных и железобетонных конструкций
Коррозия бетонных и железобетонных конструкций
Повреждения бетона отмечаются при действии на него водных растворов кислот или кислых газов, растворов солей и даже щелочей, некоторых органических соединений. Степень агрессивного воздействия зависит не только от состава агрессивной среды, но и от условий контакта, скорости движения и напора жидких сред, плотности прилегающего грунта при действии грунтовых вод, температуры среды, силовых нагрузок, напряженного состояния материала конструкций и других факторов. Степень агрессивности среды – понятие относительное по отношению к бетону. Среда может быть агрессивной по отношению к бетону на портландцементе и неагрессивной по отношению к бетону такого же состава на глиноземистом или шлакопортландцементе, степень агрессивности будет различна к бетонам разной плотности. Коррозионные процессы в твердой и газообразной средах фактически начинаются и протекают только в присутствии жидкой фазы. Атмосферные воды, выпадающие в виде осадков, содержат обычно ничтожное количество солей: хлор-ионов, сульфатов в расчете на SO3 и некоторое количество растворенной СО2. Количество SO3 может быть значительно больше в городах, загрязненных дымовыми газами. Перенос солей в приморских районах и туманообразная влага обусловлены сильными ветрами. Химический состав речной воды зависит от источников питания реки и вида пород, через которые она фильтруется. Если вода пополняется в реке за счет осадков, то она мало минерализована и имеет малую степень жесткости. При питании грунтовыми водами степень ее минерализации значительна. Промышленные жидкие агрессивные среды очень разнообразны. Они подразделяются на органические и неорганические. Наиболее опасны для бетона кислые агрессивные среды. Специфически действуют на бетон жидкие углеводороды. Проникая в поры бетона, они вытесняют воду с поверхности минералов цементного камня и в зависимости от своей вязкости, летучести или испаряются в последующем (при этом цементный камень восстанавливает свои свойства), или остаются в порах цементного камня (масла), что приводит к понижению его прочности.
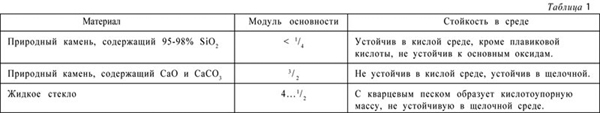
Обычная воздушная среда не агрессивна по отношению к затвердевшему плотному бетону. Агрессивность газовой среды значительно повышается с содержанием в атмосфере углекислоты, солей морской воды, сероводорода, кислых газов (табл. 2).
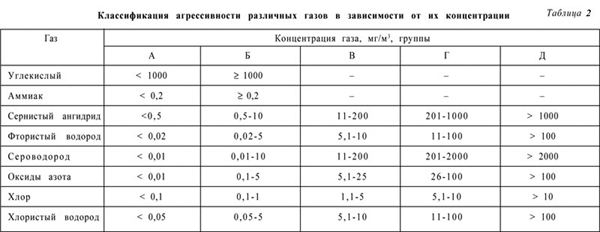
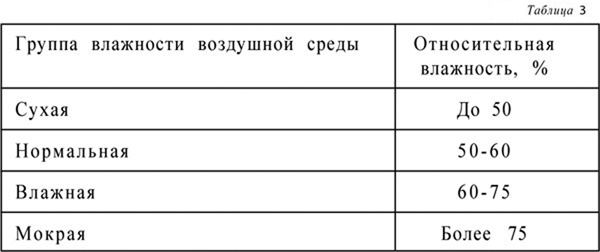
При сухом и холодном климате по сравнению с теплым и влажным коррозия металла значительно замедлена. В зависимости от степени агрессивности газы подразделяются на пять групп. При наличии в агрессивной среде нескольких газов степень агрессивности принимают по наиболее агрессивному газу. Агрессивность газов по отношению к конструкциям возрастает от группы А до Д и зависит от относительной влажности воздушной среды, в которой эксплуатируется элемент здания. В связи с этим различают следующие группы влажности воздушной среды при температуре 12-24 °C (табл. 3):
К твердым агрессивным средам относятся сухие минерализованные грунты и различные сыпучие химические материалы: удобрения, краски, гербициды, инсектофунгициды. Агрессивность твердых сред зависит от количества и состава содержащихся в них солей, условий увлажнения и влажности климата. Конденсация влаги в порошкообразном материале обусловлена двумя факторами: ее капиллярной конденсацией в промежутках между частицами порошка и гигроскопичностью материала, т.е. способностью к влагообмену с газовой средой. Гигроскопичные твердые материалы сами создают жидкую фазу, образующуюся за счет влаги воздуха. Степень агрессивности твердых тел находится в прямой зависимости от их гигроскопичности. Твердые среды в виде пыли оседают на поверхности строительных конструкций. Коррозионные процессы между твердыми агрессивными средами и бетоном возможны при появлении жидкой фазы.
Прежде чем говорить подробнее о коррозии бетона, следует сказать о главном составляющем бетона – цементном камне. Наиболее широко в строительстве применяется портландцемент и его производные: пуццолановые портландцементы и шлакопортландцементы. Под общим названием «портландцемент» подразумевается заводской продукт, имеющий в своем составе различное соотношение минералов, составляющих портландцементный клинкер. По минеральному составу цементный клинкер на 75 % состоит из силикатов кальция (трехкальциевого 3СаО•SiO2, сокращенно записываемого С3S и именуемого алитом, – 45-60 % и двухкальциевого 2СаО•SiO2, сокращенно записываемого С2S и именуемого белитом, – 20-30 %); трехкальциевого алюмината 3СаО•Al2O3(10-12)H2O, обозначаемого С3А, – 5-12 %; алюмоферритной фазы 4СаО Al2O3 Fe2O3, обозначаемого С4АF, –10-20 %; стекловидной фазы – 4-15 %; СаО свободного – до 0,5-1 %; MgO – 1-5 %; Na2O+ K2O – 0,5-1 %. В качестве заполнителей в бетоне наряду с традиционными щебнем и гравием из изверженных и плотных карбонатных пород все большее применение находят искусственные пористые заполнители: керамзит, аглопорит, шлаковая пемза, природные пористые заполнители из литоидной пемзы, перлита, шунгизита и др. Шире стали использоваться слабые известняки и отходы горной промышленности. В условиях действия кислых газов или жидкостей карбонатные породы могут разрушаться. Для воспринятия растягивающих усилий бетоны армируются стальными сетками, каркасами, стержнями. Коррозионное разрушение стали может быть в виде сплошной коррозии, которая охватывает всю поверхность металла и бывает равномерной или неравномерной по глубине, или местной коррозии, поражающей лишь отдельные участки поверхности металла (пятна, язвы, коррозионные трещины) (табл. 4, 5).
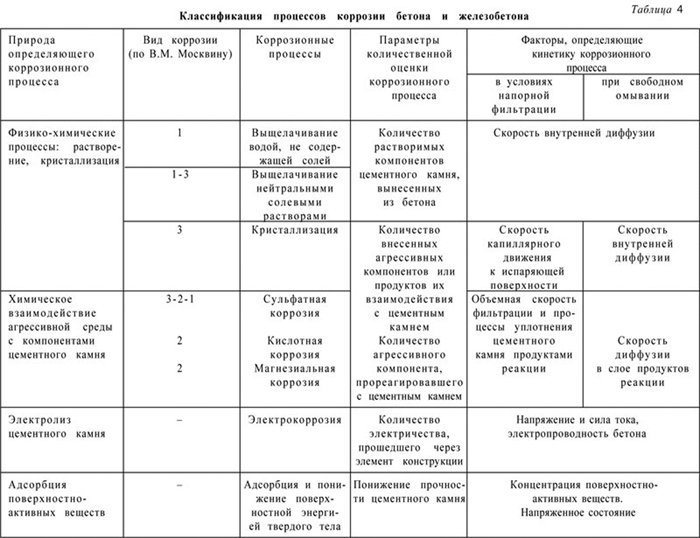
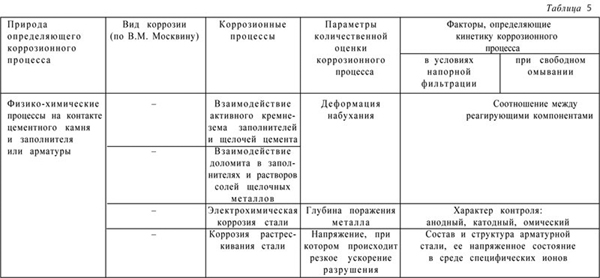
Коррозия бетона подразделяется на три основных вида:
1. Коррозия выщелачивания – все процессы, которые возникают в бетоне при действии жидких сред, способных растворять компоненты цементного камня. Составные части цементного камня растворяются и выносятся из структуры бетона. Особенно интенсивно эти процессы могут протекать при фильтрации воды через толщу бетона. Если в воде содержатся соли, не реагирующие непосредственно с составными частями цементного камня, они могут повысить растворимость гидратированных минералов цементного камня вследствие повышения ионной силы раствора. Этот вид коррозии называют «белой смертью» бетона. Действительно, поверхность бетона, покрытая белыми отложениями, образовавшимися в результате карбонизации гидроксида кальция, вынесенного из толщи бетона, свидетельствует о процессах разрушения, идущих в глубине конструкций:
Ca(OH)2 + СO2 = CaСO3 + H2O.
СаСО3 образуется в поверхностном слое в результате карбонизации гидроксида кальция глубинных слоев бетона, диффундирующего к поверхности.
Это признак растворимости компонентов цементного камня, но оценить степень опасности процесса разрушения можно только на основе тщательного анализа условий взаимодействия воды и бетона, интенсивности фильтрации воды, размеров (толщины) конструкции, изменения скорости фильтрации во времени и других обстоятельств. Стойкость к коррозии 1-го вида в значительной степени зависит от структуры и плотности цементного камня и бетона в целом. Повышение температуры и длительности твердения бетона в условиях высокой влажности улучшает его коррозионную стойкость.
2. Процессы, при которых происходят химические взаимодействия (обменные реакции) между компонентами цементного камня и раствора, в том числе обмен катионами (или обменные реакции между кислотами и солями окружающей среды и составными частями цементного камня). Образующиеся продукты реакции или легкорастворимы и выносятся из структуры в результате диффузии или фильтрационным потоком, или отлагаются в виде аморфной массы, не обладающей вяжущими свойствами и не влияющей на дальнейший разрушительный процесс (растворы кислот и некоторых солей). Коррозия 2-го вида идет в поверхностных слоях бетона. Если новообразования, не обладающие вяжущими свойствами и достаточной плотностью, чтобы воспрепятствовать дальнейшему проникновению агрессивной среды, растворяются или смываются механически, то обнажаются более глубокие слои бетона. Последние также разрушаются, и процесс коррозии протекает до полного разрушения всего бетона, однако скорость этого процесса может быть различной. Обменные реакции чаще всего протекают в бетоне под действием углекислых вод (углекислотная коррозия); под действием сернокислых и хлористых солей. Сернокислый и хлористый магний взаимодействуют с гидратом окиси кальция по схеме:
Ca(OH)2 + MgSO4 + 2H2O = CaSO4 • 2H2O + Mg(OH)2;
Ca(OH)2 + MgCl2=CaCl2 + Mg(OH)2,
где CaSO4•2H2O – двуводный гипс.
Кроме того, сернокислый магний, вступая в реакцию с трехкальциевым гидроалюминатом, разлагает его с выделением гидрата окиси алюминия
3СаОAl2O36H2O + 3 MgSO4 + 6H2O = 3 (CaSO4 • 2H2O)+ + 3Mg (OH)2 + 2Al (OH)3.
Коррозия возникает также при действии на бетон сернокислого натрия:
Са (OH)2 + Na2SO4 +2H2O = CaSO4 (2H2O +2NaOH).
Гидрат окиси натрия – хорошо растворимое вещество, оно легко размывается водой из цементного камня.
Реакция цементного камня в среде Са(OH)2 с MgСl2 протекает по схеме: Са (OH)2 + MgСl2 = СаСl2+ + Mg (OH)2.
При большой концентрации MgСl2 (выше 2 %) его реакционная емкость настолько велика, что поступающее за счет диффузии количество гидрата окиси кальция становится недостаточным. Раствор хлористого магния проникает в глубь бетона через пленку гидрата окиси магния: приходя в соприкосновение с гидросиликатом и другими гидратами, он полностью разрушает их.
Содержание ионов Сl- и SO42- в воде – среде для бетона – должно быть ограниченным. При этом допустимое количество сульфатов возрастает с увеличением концентрации хлоридов, так как при этом учитывают более высокую растворимость гипса и гидросульфоалюмината кальция; с другой стороны, объясняется это тем, что ион хлора переводит трехкальциевый гидроалюминат в труднорастворимый гидрохлоралюминат кальция. Действие солей, содержащих ионы SO42- и Сl- не всегда бывает разрушающим. При обменных реакциях в случае небольшой концентрации указанных ионов цементный камень уплотняется, его фильтрующая способность снижается вследствие отложения в порах цементного камня новообразования сернокислого кальция, гидрата окиси магния, а также сульфоалюминатных соединений.
На практике нередко происходит также коррозия бетона под воздействием углекислых вод. Углекислота содержится в громадном большинстве природных вод. Лишь при рН > 8,5 количество ее в воде становится практически не ощутимым. Биохимические процессы, протекающие и в самой воде, и в почве служат источниками обогащение СО2 природных вод. В начале растворения цементного камня углекислота взаимодействует с Са(ОН)2 и образует СаСО3: Са(ОН)2 +СО2 = СаСО3 +Н2О.
Этот процесс в начальный период имеет для бетона положительное значение, так как хорошо растворимый Са(ОН)2 переходит в труднорастворимый СаСО3. Вода, в которой углекислота и ионы Н+, НСО-3 и СО2-3 находятся в равновесии, не способна растворить карбонатную пленку бетона. При увеличении же содержания СO сверх равновесного вода растворяет карбонатную пленку. При содержании СО2 в воде порядка 280-300 мг/л при реакции с ней образуется бикарбонат СаСО3 + СО2 + Н2О = Са (НСО3)2, который хорошо растворяется и вымывается водой из цементного камня. По мере уменьшения количества агрессивной СО2 скорость реакции затухает.
На поверхности цементного камня образуется карбонизированный слой, имеющий небольшую толщину, который под действием агрессивного раствора разрушается. В то же время гидрат окиси кальция диффундирует из глубинных слоев бетона. Появление ионов ОН изменяет установившееся равновесие и переводит в осадок бикарбонат в виде карбоната кальция. Появившийся в растворе гидрат окиси кальция связывает СО2 и образующийся карбонат выпадает в осадок.
Карбонатный слой разрушается до тех пор, пока скорость диффузии не сравняется со скоростью углекислой коррозии карбонизированного слоя либо когда начнут разрушаться гидратированные элементы цементного камня. При появлении избытка ионов ОН на поверхности цементного камня вначале образуется карбонат кальция, который затем переходит в раствор в виде бикарбоната.
Отсюда становится понятным, почему на железобетонных конструкциях виден хорошо выраженный карбонизированный слой толщиной в несколько миллиметров в надводных частях сооружения. В частях, находящихся под действием воды, содержащей агрессивную углекислоту, толщина карбонизированного слоя составляет лишь доли миллиметра. При быстром движении воды равновесие в растворе не устанавливается. Скорость коррозии замедляется из-за уменьшения реагирующей поверхности. При разрушении цементного камня на поверхности бетона остаются зерна заполнителя. Если зерна достаточно стойки против действия углекислых вод, они препятствуют проникновению агрессивной среды – воды – в более глубокие слои бетона.
При фильтрации воды, содержащей агрессивную углекислоту, через бетон можно наблюдать развитие коррозионных процессов по следующей схеме:
– постепенное насыщение бикарбонатом кальция и, как следствие, разрушение цементного камня (бикарбонат уносится водой);
– насыщение раствора бикарбоната встречающимся на пути гидратом окиси кальция и выпадение в осадок карбоната кальция (зона уплотнения);
– растворение цементного камня фильтрующей водой, лишенной полностью углекислоты.
Интенсивное разрушение бетона начинается тогда, когда граница зоны разрушения достигнет безнапорной грани бетона. До этого момента уплотнение внутренних слоев бетона несколько снижало эффект разрушения от действия агрессивной углекислоты.
3. Процессы, при развитии которых в порах и капиллярах бетона происходят накопление и последующая кристаллизация малорастворимых продуктов реакции с увеличением объема твердой фазы или веществ, способных при фазовых переходах, полимеризации и тому подобных процессах увеличивать объем твердой фазы в порах бетона. В бетоне возникают внутренние напряжения, которые приводят к повреждению его структуры. К этому виду относится коррозия при действии сульфатов. Микро- и макроструктура цементного камня, раствора и бетона играет значительную роль в развитии процессов коррозии третьего вида. Большое значение имеет взаимное расположение и абсолютные размеры открытых и закрытых капилляров и пор, однородность структуры.
Для обеспечения нужной удобоукладываемости бетона при его изготовлении вводится избыток воды. На процессы гидратации цемента, водопоглощение заполнителей требуется не более 20-30 % взятой воды. Остальная же вода, находящаяся в бетоне в свободном состоянии, образует при дальнейшем твердении бетона поры и капилляры.
Крупные пустоты, сообщающиеся между собой и с поверхностью, служат путями для проникновения агрессивных растворов. Закрытые поры играют отрицательную роль, когда развивается осмотическое давление. Мелкие пустоты заполняются продуктами гидролиза и гидратации, в первую очередь гидратом окиси кальция.
В процессе развития коррозии третьего вида структура бетона претерпевает значительные изменения. Уменьшается пористость, появляются трещины параллельно поверхности, заполненные преимущественно гипсом или гипсом и сульфоалюминатом кальция. Трещины развиваются, как правило, на участках цементного камня с высоким содержанием гидрата окиси кальция и с менее однородной структурой. Одновременно с увеличением ширины и глубины трещин их стенки разрушаются.

Разрушение в этом случае происходит из-за роста кристаллов гидросульфоалюмината кальция, кристаллизации солей при наличии испаряющейся поверхности для конструкций, частично погруженных в раствор соли, полимеризации мономера с увеличением объема. Образовавшийся на первой стадии двуводный гипс CaSO4•2H2O реагирует затем с трехкальциевым гидроалюминатом, образуя труднорастворимый гидросульфоалюминат кальция, который увеличивается в объеме примерно в 2,5 раза. Кристаллы гидросульфоалюмината кальция представляют собой длинные тонкие иглы, напоминающие бациллы (3СаО•Al2O3 + +3CaSO4 + 31H2O = 3CaO•Al2O3•3CaSO4•31H2O). Вследствие такого сходства и за весьма разрушающее воздействие гидросульфоалюминат кальция назван «цементной бациллой». В начале отложения гипса в порах образуется гидросульфат кальция, приводящий к уплотнению бетона. По этой причине иногда не удается распознать начальные формы коррозии третьего вида. Такое уплотнение бетона создает картину ложного благополучия. Хотя прочность бетона вначале растет, но после возникновения больших растягивающих напряжений в стенках пор и капилляров, вызванных ростом кристаллических новообразований, она резко снижается и происходит разрушение структурных элементов бетона.
Продолжительность состояния «благополучия» зависит от плотности и прочности бетона. Для плотных и прочных бетонов это состояние может длиться несколько лет, поэтому надо быть очень осмотрительным при оценке условий возникновения коррозии третьего вида. Скорость ее зависит от концентрации сульфатов в воде, минералогического состава клинкера и от микро- и макроструктуры цементного камня.
С увеличением содержания С2S уменьшается концентрация Са(ОН)2 и сульфатостойкость увеличивается, так как гидроалюминат при пониженной концентрации Са(ОН)2, реагируя в растворенном виде с сульфатом кальция, не вызывает разрушения цементного камня. При повышенном содержании С3S увеличивается концентрация Са(ОН)2. При высокой концентрации Са(ОН)2 реакция между С3А и гипсом происходит в твердой фазе, так как гидроалюминат в насыщенном известковом растворе растворяться не может. В результате этой реакции образуются кристаллы гидросульфоалюмината кальция, которые, сильно увеличиваясь в объеме, производят большие разрушения. С повышением содержания С3S стойкость цементного камня возрастает вследствие более быстрого твердения и уплотнения цементного камня и более трудного проникновения сульфатных вод в его глубину. С увеличением содержания С3А сульфатостойкость цемента снижается, и становится тем ниже, чем выше концентрация сульфатов в воде.
Повышение содержания С3А вдвое (с 5 до 10 %) увеличивает деформацию образцов. С дальнейшим ростом содержания С3А резко возрастает сульфатная коррозия, поэтому при изготовлении сульфатостойкого цемента содержание С3А в клинкере должно быть не более 5 %.
Каждому из трех видов коррозии соответствует определенная форма разрушения бетона и определенные мероприятия по его защите. Кроме этих видов существуют еще осмотическая и газовая коррозии бетона. Под действием сил осмоса вода проникает в бетон, вызывая осмотическую коррозию цементного камня. В порах последнего создается осмотическое давление, вызывающее в стенках пор напряжения. Осмотическое давление возникает в том случае, когда два раствора, отличающиеся концентрацией растворенного вещества, разделены полупроницаемой перегородкой. Полупроницаемыми материалами (цементный камень полупроницаем) называют такие, которые пропускают молекулы растворителя и не пропускают растворенное вещество. Основной метод защиты бетона от развития в нем осмотического давления – уменьшение концентрации гидрата окиси кальция. Для этого применяют белитовые цементы или цементы с активными минеральными добавками, связывающими Ca(OH)2 в труднорастворимые соединения. Под действием осмоса растворитель, стремясь выровнять концентрации, проникает через полупроницаемую перегородку из раствора с меньшей концентрацией в раствор с большей концентрацией.
Если более концентрированный раствор находится в замкнутом пространстве, заполняя его целиком, то внутри него создается давление, стремящееся разорвать стенки ячейки. Это давление уравновешивает осмотическое давление растворителя, который стремится проникнуть в ячейку. Оно может достигать нескольких атмосфер. Цементный камень полупроницаем и может вызвать осмотическое давление, если он разделяет водные растворы различной концентрации. Кроме того, в порах цементного камня всегда содержится свободный гидрат окиси кальция в виде раствора значительной концентрации, а также и другие растворенные вещества. Концентрация раствора гидрата окиси кальция в порах цементного камня всегда будет выше, чем в пресной воде. В результате вода начнет проникать в поры цементного камня, создавая в них осмотическое давление. Развитие осмотического давления от нуля до максимума в водных условиях и от максимума до нуля в последующих воздушно-сухих условиях должно оказывать особенно сильное коррозионное воздействие на бетон, подверженный периодическому увлажнению и высушиванию, например на бетон в зонах переменного уровня воды в гидротехническом сооружении. Основной метод защиты от осмотического давления – уменьшить концентрацию гидрата окиси кальция.
При взаимодействии газов с бетоном образуются соли кальция. Наиболее существенно на свойства нейтрализованного бетона влияют растворимость и гигроскопичность образующейся соли, объем новообразований относительно исходных подвергающихся нейтрализации минералов, агрессивность соли по отношению к стальной арматуре. Газы разделяются на следующие группы:
Первая группа – газы, образующие практически нерастворимые и малорастворимые соли кальция (газы: двуокись углерода, фтористый водород, фтористый кремний, фосфорный ангидрид, пары щавелевой кислоты). Эти соли или совсем не содержат кристаллизационной воды или содержат незначительное количество. Объем твердых фаз в цементном камне при его химическом взаимодействии с газами в большинстве случаев увеличивается, а проницаемость бетона обычно уменьшается. Из числа распространенных газов лишь фтористый водород взаимодействует с Са(ОН)2 с уменьшением суммарного объема твердых фаз. Малая растворимость этих солей практически исключает их диффузию в глубь бетона. Прочность нейтрализованного бетона мало зависит от его влажности. Повреждение железобетонных конструкций при действии газов первой группы наступает вследствие коррозии арматуры после нейтрализации защитного слоя бетона.
Вторая группа – газы, образующие слаборастворимые соли, содержащие более или менее значительное количество кристаллизационной воды, что сопровождается большим увеличением объема твердых фаз и уплотнением бетона (газы: сернистый и серный ангидрид, сероводород). Дальнейшее проникновение газа может прекратиться, однако возникающие при этом большие внутренние напряжения могут вызвать послойное разрушение бетона. Диффузия малорастворимых солей в глубь бетона сильно ограничена, поэтому коррозия стальной арматуры в атмосферных условиях наблюдается лишь в нейтрализованном слое. При увлажнении конструкции объем кристаллогидратов может возрасти, в результате чего повысятся внутренние напряжения и в конечном счете понизится прочность бетона. Железобетонные конструкции в присутствии газов второй группы повреждаются вследствие коррозии стальной арматуры после нейтрализации защитного слоя, а в средах с высокой влажностью также из-за уменьшения прочности и послойного разрушения бетона.
Третья группа – газы, образующие хорошо растворимые и гигроскопичные соли. При повышении влажности воздуха гигроскопичные соли, поглощая водяной пар, образуют растворы, которые за счет капиллярного всасывания и диффузии в жидкой фазе способны проникать в глубь бетона. В результате растворения кальциевых солей или их кристаллизации с большим увеличением объема твердой фазы прочность поверхностного слоя бетона вначале может увеличиться, а затем уменьшиться, т. е. происходит его постепенное разрушение. Образующиеся соли могут быть агрессивными или нейтральными по отношению к арматуре, поэтому газы этой группы делят на две подгруппы. входят газы (галогенсодержащие: хлористый водород, хлор, двуокись хлора, а также пары брома и йода, монохлоруксусной кислоты), образующие соли, способные уже в малой концентрации вызывать коррозию стали в жидкой фазе бетона, имеющей щелочную реакцию, т. е. до нейтрализации защитного слоя. входят газы (окислы азота, пары азотной кислоты), которые дают хорошо растворимые кальциевые соли, не вызывающие коррозии стали в щелочной среде бетона. При высокой влажности среды и возможности выноса образующихся солей из бетона, например при периодических обливах конструкции или образовании конденсата на поверхности бетона, газовую коррозию трудно отличить от коррозии 2-го или 3-го вида в жидких средах, идущей до полного разложения основных минералов цементного камня с образованием кислых солей и послойным разрушением бетона.
Все кислые газы действуют на бетон конструкций совместно с СО2. В большинстве случаев опережающим процессом является карбонизация бетона, которая начинается с момента изготовления конструкции, тогда как специфические кислые газы начинают действовать, как правило, лишь после начала эксплуатации здания. Воздействие газов на бетон вызывает его нейтрализацию, а образующиеся соли проникают вглубь со скоростью, зависящей от их растворимости, проницаемости и влажности бетона. Совместное действие, например, углекислого газа и фтористого водорода, приводит к переходу карбоната кальция во фтористый кальций, в результате уменьшается объем твердых фаз и, следовательно, увеличивается проницаемость бетона, что способствует ускорению карбонизации.
В естественных условиях редко встречается коррозия только одного вида, но всегда можно выделить преобладающее действие какого-либо вида, а затем проследить и учесть роль вторичных для данного случая видов коррозии. Капиллярно-пористая структура цементного камня в бетоне (его высокоразвитая внутренняя поверхность) в значительной мере определяет интенсивность взаимодействия (коррозионных процессов) между внешней средой и бетоном. Под структурой твердого материала понимают соотношение расположения в пространстве отдельных первичных элементов и характеристики сил, соединяющих эти элементы. Наиболее элементарным (первичным) уровнем является атомно-молекулярный уровень структуры компонентов, составляющих бетон. Такие свойства, как растворимость в воде, способность реагировать с водой или в контакте с ней, термическая устойчивость в интервале температур, реакционная способность по отношению к различным классам химических соединений, проявляются на молекулярном уровне. На втором уровне сложности структуры (на уровне первичных частиц-микрокристаллов или аморфных частиц) появляется поверхность раздела фаз. Возникают такие свойства, как прочность, плотность. Свойства поверхности минералов цементного камня определяют его поведение по отношению к жидкостям различной полярности, к растворам поверхностно-активных веществ. На третьем уровне сложности структуры появляются образования, состоящие из многих частиц, и поровое пространство. Именно в поровом пространстве развиваются коррозионные процессы. На четвертом уровне сложности структуры (на уровне элементов конструкций) в агрессивных средах проявляется влияние таких факторов, как размеры конструкции, образование неравномерного поля напряжений из-за различной скорости коррозионных процессов в разных частях конструкций или из-за неоднородности температурного поля. Все поры в бетоне можно классифицировать по месту нахождения в его объеме на три вида: поры цементного камня (гелевая составляющая – тонкодисперсная часть и крупные поры), поры заполнителя и контактные поры на поверхности раздела цементного камня и заполнителя.
С. Д. СОКОВА, профессор МГСУ











